重磅|石药集团发布mRNA-LNPs的创新制备方法
Author: Mika Huang Date: September 3, 2024
mRNA脂质纳米颗粒(mRNA-LNPs)技术面临的主要挑战是储存条件的问题。此前已获批的辉瑞/BioNTech公司的mRNA疫苗需存储在-60℃~-80℃,而Moderna公司的mRNA疫苗则需要存储在-15℃~-25℃。虽然研究者开展了大量的体内研究,但在解决mRNA-LNPs体外稳定性差的问题上仍收效甚微,面临的问题主要包括颗粒聚集,mRNA氧化水解,以及反复冻融引起的不可逆相变等。
mRNA-LNPs的诸多理化性质直接影响和决定着下游的生物活性和安全性,包括形态、粒径分布、空壳占比、存储稳定性以及转染效力等,而这些性质的优劣则严重依赖于制备方法。因此,开发一种大规模、高质量、可稳定存储的mRNA-LNPs制备方法就显得尤为重要。
近期,国内mRNA疫苗先锋石药集团的研究团队在Journal of Controlled Release发表了题为"A preparation method for mRNA-LNPs with improved properties"的研究性论文。该研究发现:在制备过程中,采用两步切向流过滤(tangential-flow filtration, TFF)方法可有效改善mRNA-LNPs的诸多理化性质,特别是在空包率、储存稳定性、转染效率以及体内分布方面。这些改进在优化其工业适用性和扩大其临床应用等方面展现了巨大的潜力。

01 TFF法技术路径
mRNA-LNPs由编码致病抗原的mRNA,脂质混合物以及缓冲液组成。具体来说,mRNA-LNPs是通过将溶解在乙醇中的脂质与溶解在pH为4.0的水性缓冲液中的mRNA快速混合,然后在透析液中透析或TFF结合过滤除菌来制备的。其中,TFF环节被认为是LNPs形成的关键步骤,因为它不仅移除了乙醇,而且还可以通过提高pH促进LNP颗粒的融合。传统的一步法TFF利用pH=7.6的缓冲溶液,通过提高pH直接实现乙醇的去除和mRNA-LNPs的融合;而两步法TFF则先使用pH=4.0的缓冲液经TFF置换去除乙醇,随后第二步TFF过程中使用pH=7.6的缓冲液制备获得mRNA-LNPs。

图1. mRNA LNPs的制备方法示意图
02 TFF过程乙醇的影响
-
粒径、空包率对比
采用DLS、dCryo-EM和NanoFCM等方法,对三种不同的阳离子脂质(SM102, ALC-0315和Dlin-MC3-DMA)和不同制备方法(一步法TFF和两步法TFF)的所得mRNA-LNPs的大小、形貌和空包率进行了深入分析。两步TFF制备方法获得的mRNA-LNPs粒径显著大于一步TFF所得LNPs,Cryo-TEM的结果与DLS一致(图3a)。此外,结合SYTO13核酸染色,使用NanoFCM对空包率进行检测。待测颗粒通过NanoFCM探测区时,同时获得侧向散射SS和荧光FL的信号,有SS信号无对应的FL信号的颗粒为空的LNP,在二维散点图中,mRNA LNPs和Empty LNPs清晰地分成两个群体(图2b),基于纳米流式检测技术仅需1min即可实现mRNA-LNPs样本中空包率的准确定量(图3b和表1)。结果表明,两步法TFF产生的mRNA-LNPs颗粒粒径更大、空包率更低同时形态更加均匀。

图2. NanoFCM对mRNA-LNPs的空包率表征
表1. 三种阳离子脂质经一步TFF和两步TFF合成所得mRNA-LNPs的空包率

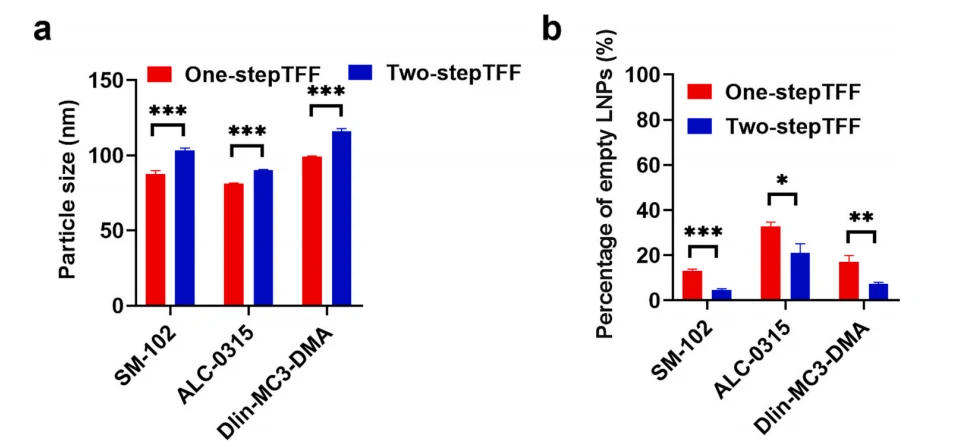
图3. 不同制备方法所得mRNA LNPs的粒径和空包率
-
颗粒融合分析
如图4所示,作者从粒径、形态、包封率和空包率等维度,进一步阐明了两种制备方法颗粒融合过程中有无乙醇)对颗粒融合的影响。选取SM-102阳离子脂质为研究模型,结果显示:在经过TFF之前,有机相和水相混合后的mRNA-LNPs粒径在59.7 nm,空包率73%;经过一步TFF后粒径增加且稳定在87 nm左右,空包率下降到13.0% (图4a和4f);而在两步TFF处理过程中,第一步TFF后乙醇残留小于1.0%,导致LNP发生了轻微的融合,其粒径和空包率分别为74.4 nm和64.3%,第二步TFF后随着pH增高,粒径从74.7 nm增加到102.5 nm,LNP空包率则降低至6.4%。随着TFF时间延长,LNP粒径最终维持在103 nm左右,空包率为4.5%(图4c,4f)。在其他两种类型的阳离子LNPs中也观察到了相同的现象。因此,当pH逐渐接近可电离阳离子脂质的pKa值时,颗粒会发生融合,颗粒粒径增大同时空包LNPs比例降低。更重要的是,通过两步TFF方法产生的mRNA-LNPs粒径更大,空包的LNPs更低而且形态更均匀,充分证明两步TFF方法在不同的可电离脂质配方中具有普适性。

图4. 不同制备方法所得mRNA-LNPs的粒径和空包率分析
作者进一步结合稳定性、细胞和小鼠转染等实验,从多个维度综合对比了两种制备方法所得的mRNA-LNPs。新的两步TFF方法获得的mRNA LNPs经过了完整的融合过程,因此其稳定性和下游生物活性显著提高,如转染效率增强同时心脏和血液中的分布降低。
03 展望
此前,在2022年石药集团全年业绩电话会上,在被问及新鲜获批的新型冠状病毒mRNA疫苗(SYS6006)与其他新冠疫苗对比有何优势时,本文的通讯作者李春雷博士这样回应:

从中我们不难捕捉到“调整LNP尺度”、“新技术助推空载率检测,提升递送效率”等关键信息。随着石药集团mRNA新冠疫苗的成功获批和论文的发表,相信这些对于mRNA疫苗至关重要的表征参数——载体尺寸、空载(包)率等会引起越来越多核酸药物从业者的重视。
NanoFCM基于自身的技术平台开发了一种高灵敏、快速、直接、无创的mRNA疫苗表征方法,在石药的研究中NanoFCM公司的纳米流式提供了mRNA-LNPs的空包率信息,并实现了mRNA疫苗储存稳定性的长期追踪。基于纳米流式卓越的散射和荧光灵敏度,可同时获取mRNA-LNPs的粒径、浓度、空包率、载药效率、mRNA拷贝数、靶向配体密度等多项参数的表征结果,为mRNA疫苗等核酸纳米药物的研发和质量控制提供了重要的技术保障,这将极大加快核酸疗法的基础研究和临床转化进程。

Tip:如您希望进一步获取以上文章、了解纳米流式在核酸药物的应用方案或者申请仪器试用,可扫描下方客服二维码或联系区域销售获取。

欢迎扫码关注
参考文献
-
Cong Geng, Kefan Zhou, Ying Yan, et al. A preparation method for mRNA-LNPs with improved properties[J]. Journal of Controlled Release, 2023, 364: 632–643.



